Une stratégie épigénétique contre le cancer lié à l’amiante
Les traitements actuels pour traiter certains cancers agressifs comme le mésothéliome, lié à une exposition à l’amiante, donnent des résultats cliniques décevants. En quête de nouvelles voies, des chercheurs de l’Institut de chimie des milieux et matériaux de Poitiers (CNRS/Université de Poitiers), en collaboration avec une équipe nantaise du Centre de recherche en cancérologie Nantes-Angers (INSERM/CNRS /Université de Nantes/Université d’Angers) et une équipe du Laboratoire de chimie des polymères organiques de Bordeaux (CNRS/Université de Bordeaux) ont développé une approche originale utilisant des nanovecteurs actifs sur des cibles épigénétiques. Résultat : une réduction de 80% de la croissance tumorale chez la souris. Ces travaux sont publiés dans la revue Theranostics.
Le mésothéliome pleural, cancer lié à l’amiante, est une forme très agressive de cancer des poumons pour lequel le traitement actuel est peu probant. Une stratégie innovante de traitement de cette pathologie proposée actuellement par la communauté scientifique repose sur les mécanismes épigénétiques de régulation de l’expression de gènes. En effet, dans les cellules cancéreuses, les gènes chargés des mécanismes du contrôle cellulaire sont rendus inopérants par un processus de « marquage » épigénétique anormal. Ce marquage anormal étant réversible, il peut être reprogrammé afin de réactiver les mécanismes normaux de régulation cellulaire-
Au cours de travaux antérieurs, les chercheurs de l’Institut de chimie des milieux et matériaux de Poitiers sont partis du constat que la formation du mésothéliome est associée à la diminution, entre autres, d’une marque épigénétique, résultant de l’activité anormale des désacétylases d’histones (HDAC) surexprimées dans la plupart des cancers. L’utilisation de molécules bloquant l’activité de ces désacétylases pourrait donc se révéler efficace en oncologie. L’équipe a ainsi développé une nouvelle molécule bloquant ces HDAC. L’efficacité de ce nouveau composé a été validée grâce à la réalisation de nombreux tests biologiques par une l’équipe du Centre de recherche en cancérologie Nantes-Angers.
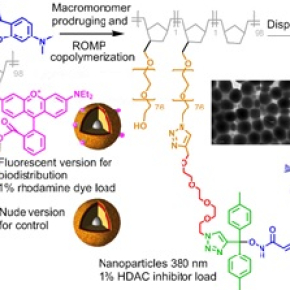
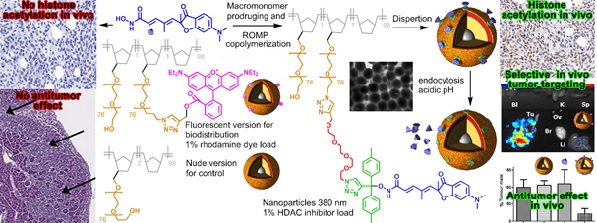
Afin de minimiser les inconvénients dus à l’utilisation in vivo de cette molécule (toxicité, métabolisme, effets secondaires, manque de sélectivité pour les organes à traiter), les chercheurs ont associé à cette stratégie épigénétique des nanovecteurs thérapeutiques à base de polymères. Ces vecteurs, élaborés par le Laboratoire de chimie des polymères organiques de Bordeaux, sont capables d’acheminer sélectivement un agent actif à l’intérieure des cellules tumorales grâce à leur fort pouvoir de pénétration. Le résultat le plus marquant a été obtenu sur un modèle murin orthotopique de mésothéliome péritonéal avec une réduction de 80% de la croissance tumorale, alors que la molécule active ou le vecteur utilisé seuls ne donnent aucun effet. Ces travaux vont maintenant se poursuivre afin d’envisager un transfert vers la clinique.
* Principaux constituants protéiques des chromosomes.
Référence
Fatima el Bahhaj, Iza Denis, Loic Pichavant, Régis Delatouche, Floraine Collette, Camille Linot, Daniel Pouliquen, Marc Grégoire, Valérie Héroguez, Christophe Blanquart & Philippe Bertrand
Histone Deacetylase Inhibitors Delivery using Nanoparticles with Intrinsic Passive Tumor Targeting Properties for Tumor Therapy
Theranostics 25 mars 2016
doi: 10.7150/thno.13725