Le neuropeptide FF: une nouvelle hormone qui protège le tissu adipeux de l’inflammation
Une collaboration internationale impliquant l’équipe de Frédéric Simonin du Laboratoire de biotechnologie et signalisation cellulaire, identifie le neuropeptide FF comme une hormone circulante. La diminution du taux plasmatique de ce peptide chez les patients obèses conduirait à l’inflammation du tissu adipeux entrainant des troubles du métabolisme et des maladies associées, telles que le diabète de type 2. Cette étude a été publiée le 5 juin 2017 dans la revue Journal of Clinical investigation.
Le tissu adipeux contient des cellules immunitaires, notamment des macrophages, qui jouent un rôle important dans son développement et le métabolisme. Chez les personnes obèses, ces macrophages s’accumulent dans le tissu adipeux et acquièrent un phénotype de type M1 favorisant une inflammation qui est en partie à l’origine des maladies métaboliques associées à l’obésité (dyslipidémies, diabète de type 2).
Les chercheurs montrent que le neuropeptide FF (NPFF), déjà connu pour ses effets dans le système nerveux central, est également présent dans la circulation sanguine, chez l’homme et la souris, à des concentrations qui sont compatibles avec une action sur son récepteur. Par ailleurs, le taux de ce peptide dans le plasma est diminué chez les obèses et il augmente lors d’une restriction calorique. Enfin, ce travail a mis en évidence la présence du récepteur de ce peptide (NPFFR2) à la surface des macrophages du tissu adipeux et montré que l’activation de NPFFR2 par le NPFF favorise le phénotype M2 (effet anti-inflammatoire) et la prolifération des macrophages du tissu adipeux. Ces effets sont absents dans les souris génétiquement déficientes pour NPFFR2 qui ont été générées et caractérisées par l’équipe de Frédéric Simonin.
D’un point de vue mécanistique, les effets du NPFF impliquent une cascade d’événements, qui conduit à l’augmentation de la phosphorylation du facteur de transcription STAT-6 avec pour conséquence une augmentation de l’expression des gènes de type M2. Par ailleurs, le NPFF favorise la prolifération des macrophages en augmentant l’expression d’un gène (Ndrg2), impliqué dans la multiplication de certains types cellulaires et en inhibant la transcription des membres de la famille Ifi200, inhibiteurs du cycle cellulaire, et de Mafb, un régulateur négatif de la prolifération des macrophages.
Dans l’ensemble, ces résultats indiquent que le NPFF représente un nouveau signal hormonal qui augmente le nombre de macrophages du tissu adipeux et maintient les macrophages nouvellement formés dans un phénotype M2 qui diminue l’inflammation des tissus adipeux (Figure). Par contre, chez les patients obèses, la diminution du NPFF circulant favoriserait la transition des macrophages vers un phénotype M1 induisant l’inflammation du tissu adipeux ce qui aurait des conséquences néfastes pour le métabolisme et les maladies associées. Le récepteur de ce peptide, NPFFR2, pourrait ainsi représenter une cible thérapeutique d’intérêt dans le traitement des maladies métaboliques associées à l’obésité.
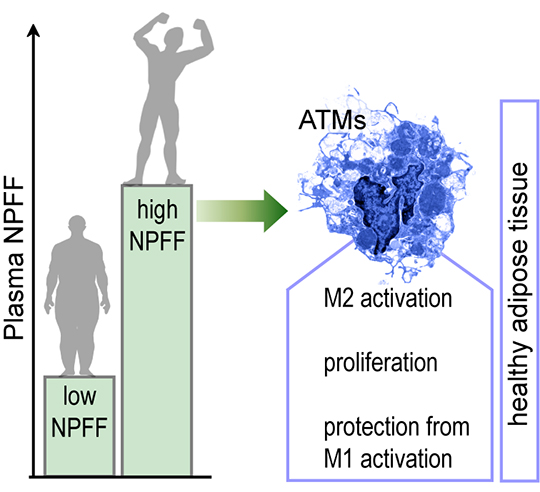
©Tamas Roszer
En savoir plus
-
Neuropeptide-FF increases macrophage self-renewal and abrogates inflammation in adipose tissue.
Waqas S.F.S., Hoang, A.C.; Lin Y.-T., Ampem, G., Azegrouz H., Balogh L., Thuróczy, J., Chen J.-C., Gerling I. C., Nam S., Lim J.-S., Martínez-Ibañez J., Real J. T., Paschke S., Quillet R., Ayachi S., Simonin F.; Schneider M., Brinkman J.A., Lamming D.W., Seroogy C. M., Röszer T.
J. Clin. Invest. 2017. Published June 5, 2017 doi:10.1172/JCI90152.