Complexité des échanges entre molécules d’ADN lors de la recombinaison
La recombinaison homologue est un mécanisme de réparation des cassures de l’ADN responsable des échanges chromosomiques lors de la méiose. Les modèles actuels n’expliquent pas la complexité des profils de recombinaison méiotique observés. Un travail collaboratif entre le Commissariat à l’Energie Atomique et le Centre de recherche en cancérologie de Marseille publié le 5 avril 2018 dans la revue Molecular Cell éclaire les bases mécanistiques et le contrôle génétique de cette complexité.
Notre vision de la recombinaison résulte de plusieurs décennies d’études de la méiose, notamment chez les champignons filamenteux et les levures. En plus du « modèle de Holliday » qui explique l’échange réciproque de deux molécules d’ADN grâce à une jonction baptisée du nom de son inventeur, un autre élément important fut le postulat puis la confirmation de la formation d’hétéroduplex au cours de la réaction. Il s’agit de régions de la molécule d’ADN (duplex) où les deux brins appariés viennent de chacun des deux parents et peuvent donc présenter des mésappariements de bases, dont la réparation s’impose et génère soit une restauration génique (maintien équilibré des copies parentales) soit une conversion (déséquilibre en faveur de l’une des copies).
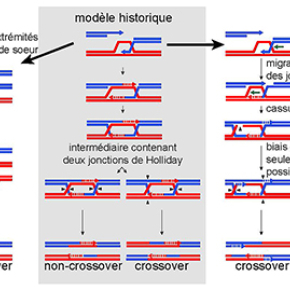
Le modèle canonique de recombinaison, publié il y a 35 ans, se fondait sur la réparation des cassures double brin de l’ADN (DSBR = Double Strand Break Repair). Ce modèle postule un mécanisme de conversion génique avec ou sans crossover (échange réciproque de bras chromosomiques) à partir du clivage différentiel d’un même intermédiaire qui contient deux jonctions Holliday liant les chromatides recombinantes (voir Figure). A ce modèle s’est ajouté le modèle d’appariement dépendant de la synthèse d’ADN (SDSA = Synthesis Dependent Strand Annealing) qui produit exclusivement des conversions sans crossover. Finalement, il a été montré que les intermédiaires à deux jonctions de Holliday pouvaient être défaits par isomérisation sous l’action combinée d’une hélicase et d’une topoisomérase. Toutefois, ces modèles n’expliquent pas toute la complexité des profils de recombinaison observés qui alternent fréquemment segments de conversion et de restauration. De plus, la fréquence relative des différentes voies de recombinaison n’est pas clairement établie.
Dans cette étude de la méiose de la levure Saccharomyces cerevisiae, les chercheurs ont combiné l’analyse des hétéroduplex associés aux conversions se produisant dans l’ensemble du génome avec la carte des cassures générées par l’endonuclase méiose-spécifique Spo11 pour en déduire la nature des intermédiaires moléculaires. Ils expliquent la complexité des profils de recombinaison observés par plusieurs propriétés sous-estimées jusqu’à présent. Alors que le modèle canonique de SDSA n’envisage l’activité recombinogène que d’une seule extrémité d’une cassure double brin de l’ADN, les auteurs montrent que les évènements de conversion sans crossovers résultent majoritairement d’évènements impliquant l’activité recombinogène des deux extrémités de la cassure. Les segments de conversions associés à ces événements de « double SDSA » sont fréquemment associés à un segment de restauration centrale qui résulte du changement de matrice lors de la phase de synthèse d’ADN réparatrice. La fréquente migration des jonctions de Holliday expliquerait en partie le décalage entre les sites de cassures de Spo11 et les cicatrices observées dans l’ADN. De plus, la présence de protéines impliquées dans la coupure des jonctions de Holliday (Mlh1, Mlh3, Exo1 et Sgs1) favoriserait la segmentation des profils de recombinaison observés. Finalement, malgré la symétrie apparente de l’intermédiaire à deux jonctions de Holliday, les auteurs révèlent un biais dans son clivage dont l’origine reste à découvrir mais qui semble lié au segment d’ADN néosynthétisé.
Ces résultats constituent une avancée majeure dans la compréhension de la dynamique de la recombinaison homologue et des facteurs qui la contrôlent. Bien que cette étude porte sur la recombinaison en méiose et implique certains facteurs spécifiques, des études récentes en mitose révèlent une forte similitude du mécanisme de recombinaison dans ces deux phases du cycle cellulaire.
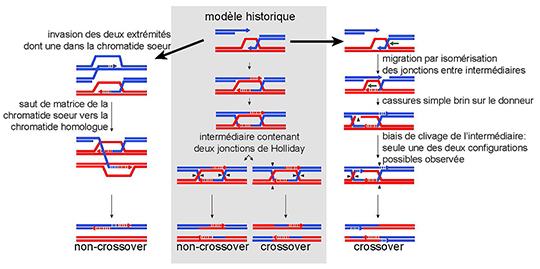
© Bertrand Llorente
En savoir plus
-
Mechanistic View and Genetic Control of DNA Recombination during Meiosis.
Marsolier-Kergoat MC, Khan MM, Schott J, Zhu X, Llorente B.
Mol Cell. 2018 Apr 5;70(1):9-20.e6. doi: 10.1016/j.molcel.2018.02.032.