Petit arrangement entre cellules : une affaire de forces
Comment les cellules régulent-elles leurs contacts pour former des structures variées, tissus et organes dont l’organisation est essentielle à la fonction biologique ? S’arrangent-elles de la même façon si elles sont du même type ou d’un type différent ? L’équipe de Pierre-François Lenne à I’Institut de biologie du développement de Marseille, a étudié comment les molécules d’adhésion et le squelette contractile des cellules déterminent la forme des contacts cellulaires dans un organe complexe, la rétine de la drosophile. Les résultats, publiés le 24 mai 2017 dans la revue eLife, mettent en lumière les rôles mécaniques directs et indirects de molécules d’adhésion et ouvrent la voie à une meilleure compréhension de certaines transformations tissulaires et de l’organisation des organes.
Dans les tissus et les organes, les cellules acquièrent différentes formes et adhèrent les unes aux autres de manière variée en fonction de leur micro-environnement et de leurs propriétés intrinsèques. Ainsi, les neurones ont des formes allongées et filamenteuses caractéristiques, connectées par des interfaces assez réduites, essentielles à l’efficacité de la transmission électrique dans un réseau complexe, tandis que les cellules épithéliales s’assemblent de manière compacte et souvent régulière, agissant comme une barrière physique et chimique avec l’extérieur.
Il y a exactement un siècle, dans son ouvrage « On Growth and Form », D’Arcy Thomson a proposé que quelques principes mathématiques et physiques généraux gouvernent la diversité des formes cellulaires, tissulaires et des organismes. Un des principes énoncés est l’existence d’une tension de surface entre cellules, grandeur physique déterminante de la forme des contacts. Nous savons aujourd'hui que la tension mécanique aux contacts cellulaires dépend de deux systèmes biologiques: d’une part, le cytosquelette, réseau actif générant des forces contractiles et d’autre part, les molécules adhésives, qui lient les cellules et les maintiennent en contact.
Comment ces deux systèmes régulent la tension mécanique est une question largement débattue. En particulier, quelle est la contribution respective de ces deux systèmes? Comment des cellules présentant des molécules d’adhésion différentes interagissent-elles et s’assemblent-elles?
Pour répondre à ces questions, l’équipe de Pierre-François Lenne étudie la rétine de la drosophile. Constituée de multiples facettes, elles-mêmes organisées en motifs cellulaires réguliers, la rétine de la mouche est un système idéal pour tenter de relier les concentrations et distributions des molécules d’adhésion et du cytosquelette aux formes et arrangements cellulaires. À chacune des interfaces entre les cellules cônes et les cellules pigmentaires (contacts homotypiques et hétérotypiques), les chercheurs ont mesuré les tensions en utilisant la nano-dissection laser, un outil capable de rompre localement les forces contractiles et d’adhésion. Les chercheurs ont observé et quantifié la concentration et la distribution des principales molécules d’adhésion dans ce système, la E- et la N-cadhérine, et celles du moteur moléculaire Myosine-II. Cette approche quantitative révèle que les forces contractiles dépendant de la Myosine-II contribuent largement à la tension, de 2 à 5 fois plus que l'adhésion. Cependant, les molécules d’adhésion, en particulier la N-cadhérine, ont un rôle indirect sur la forme, en régulant la localisation de la Myosine-II aux contacts cellulaires. Aux contacts hétérotypiques entre les cellules cônes (exprimant la E- et la N-cadhérine) et les cellules pigmentaires (n'exprimant que la E-cadhérine), les molécules de N-cadhérine ne sont pas liées. Cette asymétrie locale augmente la concentration de la Myosine-II, réduisant ainsi la surface de contact entre les cellules de type différent. En incluant ces données quantitatives dans un modèle mécanique, les chercheurs peuvent prédire les formes et arrangements des différentes cellules, dans les cas sauvage et mutants, à partir de la mesure des concentrations moléculaires aux contacts. En combinant mesures mécaniques, perturbations génétiques et modélisation, cette étude établit un lien quantitatif entre adhésion, contractilité et formes cellulaires. Il révèle également un rôle insoupçonné de la N-cadhérine dans la morphogenèse.
Ces résultats portent un éclairage nouveau sur de nombreux mécanismes biologiques, impliquant l’expression différenciée de molécules d'adhésion, parmi lesquels on peut citer le « lineage sorting », l’élimination de cellules mal spécifiées ou la transition épithélium-mésenchyme.
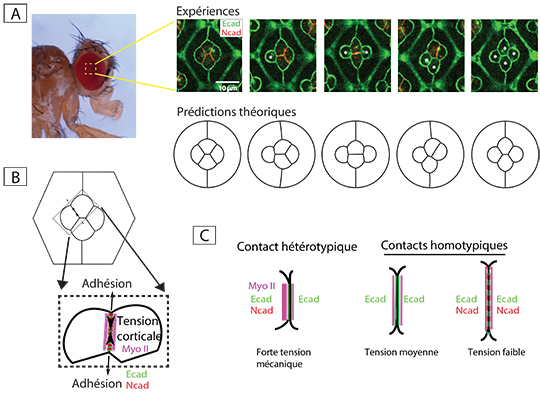
© Eunice HoYee Chan, Pruthvi Chavadimane Shivakumar, Pierre-François Lenne. eLife
En savoir plus
-
Patterned cortical tension mediated by N-cadherin controls cell geometric order in the Drosophila eye.
Eunice H.Y. Chan, Pruthvi C. Shivakumar, Raphaël Clément, Edith Laugier and Pierre-François Lenne.
eLife 2017;6:e22796. http://dx.doi.org/10.7554/eLife.22796