Une nouvelle pince moléculaire pour voir en temps réel la réparation de l’ADN
Les cassures « double-brin » peuvent entrainer de nombreuses pathologies: déficit immunitaire combiné sévère (DICS), problèmes développementaux, cancers… Dans un article paru le 21 mai 2018 dans la revue Nature Structural and Molecular Biology, une équipe interdisciplinaire de biologistes et de physiciens décrit des nouvelles méthodes nanotechnologiques permettant d’observer ces cassures en temps réel et à l’échelle d’une seule molécule. Ces approches permettent de suivre avec une résolution inégalée le déroulement temporel de la réaction de réparation de l’ADN.
En employant des méthodes de microscopie à haute résolution les chercheurs sont aujourd’hui capables d’observer et manipuler physiquement des molécules individuelles d’ADN. Ces approches permettent littéralement de tirer sur des molécules individuelles d’ADN afin de tester leur intégrité mécanique; cela est relativement aisé car les molécules d’ADN sont particulièrement longues. Or, le comportement mécanique d’une molécule d’ADN cassée est totalement différent de celui d’une molécule d’ADN intacte. Tout comme une banale corde, une molécule intacte peut résister à une force d’étirement, là où au contraire une molécule cassée n’offre aucune résistance. Les chercheurs ont développé une nouvelle molécule artificielle d’ADN qui peut ainsi être étirée afin de déterminer si elle a été réparée. Ceci leur permet de mesurer directement le temps qu’il faut pour réparer l’ADN.
En mettant cette nouvelle molécule d’ADN en présence des protéines impliquées dans la réparation des cassures double-brin chez les êtres humains, l’équipe a pu établir le rôle de chaque protéine dans le processus de réparation en passant au crible six protéines humaines qui s’assemblent en un grand complexe afin de réparer ces cassures. En analysant diverses combinaisons de ces six protéines, ils ont réussi à déterminer les règles hiérarchiques d’assemblage du complexe de réparation. Ils ont aussi pu comparer l’efficacité et la vitesse avec laquelle agissent différents complexes ou même sous-complexes de réparation. Ces travaux représentent la première caractérisation quantitative du fonctionnement des systèmes de réparation de l’ADN.
Dans des expériences actuellement en cours l’équipe commence à étudier l’effet de drogues et médicaments sur ces systèmes de réparation. En effet, les cellules cancéreuses sont marquées par une forte instabilité génétique qui les rend particulièrement dépendantes des systèmes de réparation de l’ADN. Ainsi en inhibant temporairement ces systèmes on pourrait fragiliser de façon prioritaire des cellules tumorales. Similairement, cela pourrait permettre de limiter les mécanismes de résistance aux thérapies anti-cancer existantes.
Au-delà de ces travaux sur les mécanismes de réparation de l’ADN, les méthodes mises en place par l’équipe de recherche se trouvent être généralement applicables à l’étude des interactions entre molécules médicamenteuses et leurs cibles.
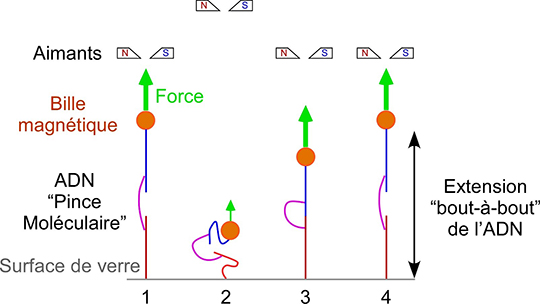
© T. Strick
En savoir plus
-
Dissection of DNA double-strand-break repair using novel single-molecule forceps.
Wang JL, Duboc C, Wu Q, Ochi T, Liang S, Tsutakawa SE, Lees-Miller SP, Nadal M, Tainer JA, Blundell TL, Strick TR.
Nat Struct Mol Biol. 2018 May 21. doi: 10.1038/s41594-018-0065-1. [Epub ahead of print]